Terapia Ormonale Oncologica:
Come Bloccare il Carburante
del Tumore
Un approccio mirato ed elegante che “affama” le cellule tumorali ormono-sensibili. Meccanismo, farmaci, effetti e strategie per viverla al meglio.
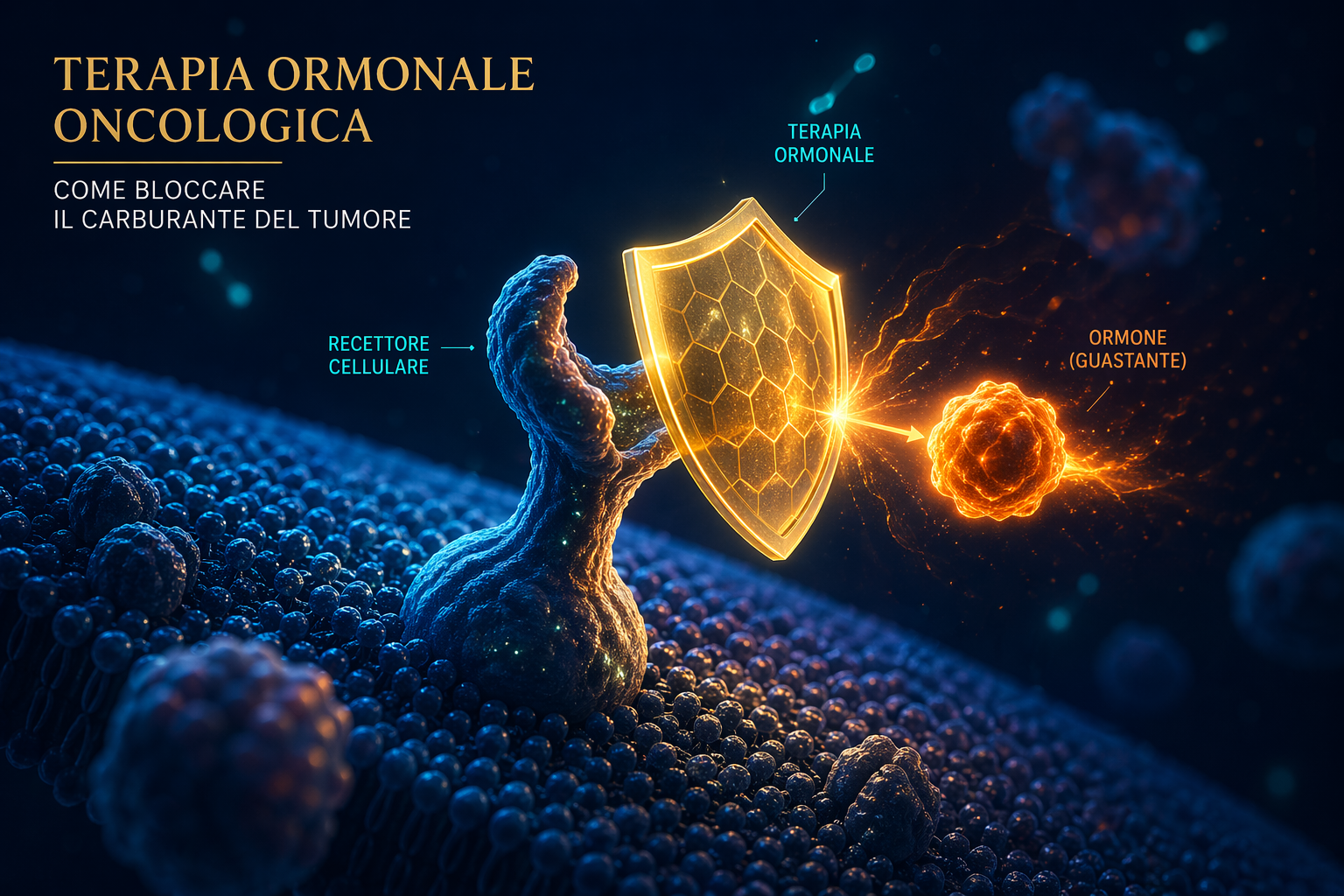
Il principio: quando il tumore usa gli ormoni come carburante
Nel vasto arsenale delle cure oncologiche, la terapia ormonale — o ormonoterapia — rappresenta una delle strategie più eleganti e mirate. A differenza della chemioterapia, non colpisce tutte le cellule in divisione: identifica e neutralizza specificamente il meccanismo che alcuni tumori usano per crescere — gli ormoni.
Tessuti come la mammella, la prostata e l’endometrio sono naturalmente sensibili agli ormoni sessuali (estrogeni, progesterone, testosterone). Le cellule tumorali che mantengono questa caratteristica usano questi ormoni come un “fertilizzante” molecolare: più ormone circola, più il tumore cresce. Privarlo di questo carburante significa fermarne la proliferazione.
Come si identifica un tumore ormono-sensibile
Il patologo analizza il campione bioptico cercando i recettori ormonali sulle cellule tumorali. Nel seno: ER (recettore degli estrogeni) e PR (recettore del progesterone). Nella prostata: AR (recettore degli androgeni). Il risultato — espresso in percentuale — determina se l’ormonoterapia è indicata e quanto è probabile che sia efficace.
Ormonoterapia vs Chemioterapia: quale differenza
Molti pazienti confondono i due approcci o temono l’ormonoterapia come se fosse chemioterapia. Sono strategie profondamente diverse — per meccanismo, tollerabilità e durata.
⚠️ Importante: non si escludono a vicenda
In molti casi, ormonoterapia e chemioterapia vengono usate in sequenza o in combinazione — ciascuna nel momento e con le modalità più appropriate. La scelta dipende dallo stadio, dalla biologia del tumore e dalle condizioni generali del paziente. Decidi sempre con il tuo oncologo, mai da solo.
I 3 meccanismi con cui l’ormonoterapia blocca il tumore
Non esiste un solo modo di “affamare” un tumore ormono-sensibile. La scienza ha sviluppato tre strategie distinte, che agiscono su bersagli diversi della catena ormonale:
Blocco del Recettore
Farmaci come il Tamoxifene si “fingono” estrogeni: occupano il recettore cellulare senza attivarlo, impedendo all’estrogeno reale di trasmettere il segnale di crescita. Come una chiave falsa che entra nella serratura ma non la apre.
Blocco della Produzione
Gli Inibitori dell’Aromatasi bloccano l’enzima che converte gli androgeni in estrogeni nel tessuto adiposo. Gli analoghi del GnRH spengono la produzione ormonale a livello ipofisario. Meno ormone prodotto = meno carburante per il tumore.
Degradazione del Recettore
Farmaci come il Fulvestrant (SERD) non si limitano a bloccare il recettore: lo degradano direttamente, riducendo la quantità di recettori disponibili nella cellula. Particolarmente utile nelle resistenze al Tamoxifene.
Terapia ormonale nel tumore al seno: i farmaci 2026
Per le pazienti con tumore al seno ER+/PR+, l’ormonoterapia è il pilastro terapeutico — spesso più importante della chemioterapia. La scelta del farmaco dipende dallo stato menopausale, dallo stadio e dal profilo molecolare.
I modulatori selettivi del recettore degli estrogeni sono il cardine del trattamento nelle donne in pre-menopausa da oltre 30 anni. Pillola orale quotidiana per 5–10 anni.
- Tamoxifene – standard di riferimento in pre-menopausa. Riduce il rischio di recidiva del 40–50% a 10 anni. Protezione ossea vantaggiosa.
- Toremifene – alternativa al Tamoxifene con profilo di sicurezza simile.
- Durata estesa (10 anni) – per pazienti ad alto rischio: ulteriore riduzione del rischio di recidiva tardiva (superiore a 5 anni dalla diagnosi).
- Combinazione con soppressione ovarica – nelle giovani ad alto rischio: analoghi del GnRH (Goserelin, Leuprolide) + Tamoxifene o inibitore dell’aromatasi.
Superiori al Tamoxifene nelle donne in post-menopausa: riducono il rischio di recidiva del 15–20% in più rispetto al Tamoxifene. Pillola orale quotidiana.
- Letrozolo (Femara) – inibitore non steroideo. Standard in adiuvanza post-menopausa e nel metastatico in combinazione con CDK4/6.
- Anastrozolo (Arimidex) – alternativa a Letrozolo, stesso meccanismo e simile efficacia.
- Exemestane (Aromasin) – inibitore steroideo: legame irreversibile all’aromatasi. Alternativa nelle resistenze.
- Switch therapy – cambio da Tamoxifene a IA dopo 2–3 anni: migliora ulteriormente la sopravvivenza.
I “degradatori” del recettore degli estrogeni sono la frontiera più avanzata dell’ormonoterapia per il seno — particolarmente efficaci nelle resistenze e nelle mutazioni ESR1.
- Fulvestrant (Faslodex) – iniezione intramuscolare mensile. Standard in seconda linea per il metastatico ER+ dopo progressione agli IA.
- Elacestrant (Orserdu) – primo SERD orale approvato FDA 2023 per ESR1-mutato: pill-based, risposta superiore alla chemio nelle pazienti pretrattate.
- Camizestrant, Imlunestrant – SERD di nuova generazione in sperimentazione avanzata: migliore biodiponibilità e attività nei tumori cerebrali.
La combinazione più rivoluzionaria dell’ultimo decennio nel seno metastatico ER+. Gli inibitori CDK4/6 bloccano la progressione del ciclo cellulare, potenziando drasticamente l’effetto dell’ormonoterapia.
- Palbociclib (Ibrance) + Letrozolo/Fulvestrant – primo approvato: raddoppia la sopravvivenza libera da progressione in prima e seconda linea.
- Ribociclib (Kisqali) + Letrozolo – unico con dimostrazione di miglioramento della sopravvivenza globale in pre-menopausa (trial MONALEESA-7).
- Abemaciclib (Verzenio) + IA – attività anche in adiuvanza ad alto rischio: approvato per il precoce con Ki-67 ≥20%. Unico CDK4/6 inibitore approvato in adiuvanza.
- Everolimus (Afinitor) + Exemestane – inibitore mTOR: per le resistenze agli IA in seconda linea.
- Alpelisib (Piqray) + Fulvestrant – inibitore PI3K per PIK3CA-mutato: bersaglio molecolare specifico con risposta significativa.
Approfondisci su ProgettoVitaSalute
→ Guida completa al tumore al seno: sottotipi, diagnosi e terapie personalizzate 2026Terapia ormonale nel tumore alla prostata: ADT e oltre
Nel tumore della prostata il testosterone è il principale motore della crescita. La Terapia di Deprivazione Androgenica (ADT) — anche chiamata “castrazione medica” — è lo standard di riferimento da decenni, oggi enormemente potenziata dai nuovi anti-androgeni di seconda generazione.
La ADT riduce il testosterone a livelli di castrazione, privando il tumore del suo principale ormone di crescita. È la base su cui si costruiscono tutte le altre terapie nella prostata avanzata.
- Analoghi del GnRH (Leuprolide, Goserelin, Triptorelina) – iniezioni mensili/trimestrali/semestrali che sopprimono la produzione ipofisaria di LH e FSH.
- Antagonisti del GnRH (Degarelix, Relugolix) – riduzione più rapida del testosterone senza il “flare” iniziale degli analoghi. Relugolix è la prima forma orale.
- Orchidectomia bilaterale – castrazione chirurgica: permanente, efficace quanto la farmacologica ma irreversibile. Raramente richiesta oggi.
La vera rivoluzione nella prostata avanzata. Questi farmaci potenziano enormemente l’ADT e hanno cambiato la storia naturale della malattia metastatica.
- Enzalutamide (Xtandi) – blocca il recettore androgenico in modo molto più efficace dei vecchi anti-androgeni. Standard nel CRPC e nel sensibile alle castrazione ad alto rischio.
- Apalutamide (Erleada) – approvato per prostata metastatica ormono-sensibile + ADT: migliora significativamente la sopravvivenza globale.
- Darolutamide (Nubeqa) – migliore penetrazione cerebrale, meno interazioni farmacologiche. In combinazione con ADT + Docetaxel nel mCSPC.
- Abiraterone (Zytiga) – inibitore della sintesi del testosterone (blocca CYP17): standard nel CRPC e in combinazione con ADT nella prostata metastatica de novo.
Anche nel tumore della prostata, le mutazioni BRCA aprono la porta ai PARP-inibitori — una delle evoluzioni più importanti degli ultimi anni nell’oncologia prostatica.
- Olaparib (Lynparza) – approvato EMA per CRPC BRCA1/2-mutato dopo progressione agli anti-androgeni di nuova generazione.
- Rucaparib (Rubraca) – alternativa in casi selezionati con mutazioni HRD.
- Olaparib + Abiraterone – combinazione approvata FDA 2023: migliora la sopravvivenza anche in pazienti senza mutazione BRCA selezionata.
- Test BRCA obbligatorio – tutti i pazienti con CRPC dovrebbero ricevere un panel genomico completo: BRCA1/2, ATM, CDK12, MSI.
Altri tumori ormono-sensibili
L’ormonoterapia non riguarda solo seno e prostata. Esistono altri tumori in cui gli ormoni giocano un ruolo importante:
Approfondisci su ProgettoVitaSalute
→ Guida completa al tumore al polmone: dalla profilazione molecolare alle terapie 2026Effetti collaterali: come riconoscerli e gestirli
L’ormonoterapia è generalmente molto meglio tollerata della chemioterapia, ma la soppressione ormonale prolungata produce effetti che richiedono attenzione attiva e gestione proattiva. Ignorarli porta a interruzioni della terapia — il peggior nemico dell’efficacia.
Molto frequenti. Gestibili con venlafaxina, clonidina, agopuntura o mindfulness. Mai interrompere la terapia senza parlarne con l’oncologo.
La soppressione estrogenica/androgenica riduce la densità ossea. MOC ogni 1–2 anni, integrazione di calcio e vitamina D, bifosfonati o denosumab se indicati.
Artriti e artralgie colpiscono fino al 50% delle donne con IA. Attività fisica regolare, fisioterapia e switch tra IA possono risolvere il problema.
Difficoltà di concentrazione e memoria. Spesso reversibile alla fine della terapia. Attività cognitiva, sonno regolare e supporto psicologico aiutano.
L’ADT nella prostata aumenta il rischio metabolico. Attività fisica aerobica regolare, dieta, controllo di pressione e colesterolo sono fondamentali.
Molto comuni in entrambi i sessi. Approccio integrato: attività fisica, supporto psico-oncologico, igiene del sonno. Non è debolezza: è biologia.
Piano di monitoraggio raccomandato durante l’ormonoterapia:
All’inizio e ogni 1–2 anni durante terapia con IA o ADT. Baseline fondamentale per monitorare la salute ossea.
Ogni 6–12 mesi nell’ADT per la prostata: rischio di sindrome metabolica aumentato. Gestione proattiva con dieta e attività fisica.
Annualmente nelle donne in terapia con Tamoxifene: raro ma possibile aumento del rischio di iperplasia endometriale. Segnalare qualsiasi perdita anomala.
Ogni 3–6 mesi nell’ADT per prostata: il PSA è il principale indicatore di risposta e progressione. Il testosterone deve confermarsi a livelli di castrazione.
Terapia prolungata per anni richiede supporto emotivo strutturato. Non è un lusso: è parte integrante del percorso di cura nei centri d’eccellenza.
Contrasta gli effetti collaterali con la biochimica giusta
La soppressione ormonale altera profondamente il metabolismo: aumenta il rischio di osteoporosi, sindrome metabolica, aumento di peso e infiammazione sistemica. Una dieta antinfiammatoria non è un optional — è uno strumento terapeutico che supporta l’osso, il metabolismo e la risposta immunitaria durante anni di terapia.
Scopri il Planner Dieta Antinfiammatoria →Le fonti scientifiche di questo articolo
Ogni affermazione è supportata da letteratura peer-reviewed e linee guida internazionali aggiornate al 2026.
- AIOM – Linee Guida Mammella e Prostata 2025
- ESMO Clinical Practice Guidelines – Breast & Prostate Cancer 2025
- ASCO 2025 – Endocrine Therapy Update (MONARCH, MONALEESA, ARCHES)
- NCCN Guidelines Breast / Prostate Cancer v2026
- PubMed – CDK4/6 inhibitors, SERD, ADT metabolic effects (2023–2026)
- Endocrine Society – Management of Hormone Therapy Side Effects 2025
Una checklist stampabile da portare in visita oncologica. Include le domande specifiche per la terapia ormonale: durata, monitoraggio osseo, effetti collaterali, combinazioni con CDK4/6, test genomici. Gratuita, senza registrazione.
Scarica la Checklist Gratuita →I migliori centri italiani per l’oncologia endocrina
Per la terapia ormonale oncologica scegli centri con oncologi specializzati in tumori ormono-sensibili, accesso ai nuovi CDK4/6 inibitori e SERD orali, laboratorio di genomica molecolare e trial clinici attivi.

FAQ
La risposta dipende dalla presenza di specifici recettori sulla superficie delle cellule tumorali. Attraverso l’esame immunoistochimico (IHC) eseguito sulla biopsia, l’oncologo verifica se il tumore è “ormono-sensibile” (es. ER+ o PR+). Se questi recettori sono presenti, il tumore usa gli ormoni come carburante e la terapia ormonale sarà efficace nel bloccarne la crescita.
No. A differenza della chemioterapia, che attacca tutte le cellule che si dividono rapidamente (comprese quelle sane), la terapia ormonale è una “terapia mirata”. Agisce solo sui segnali ormonali specifici che alimentano il tumore. Per questo motivo ha un profilo di effetti collaterali diverso e, solitamente, è meglio tollerata nel lungo periodo.
Nel contesto adiuvante (dopo l’intervento chirurgico), la terapia ormonale ha solitamente una durata che va dai 5 ai 10 anni. Questa tempistica è necessaria per ridurre al minimo il rischio di recidiva, mantenendo il tumore “affamato” e silente per un periodo di tempo prolungato.
No. Sintomi come vampate, dolori articolari o stanchezza tendono a persistere durante il periodo di assunzione del farmaco, ma solitamente scompaiono o si attenuano drasticamente una volta terminata la terapia. Molti di questi effetti possono essere gestiti con successo attraverso lo stile di vita, il movimento e la nutrizione specifica.
Il Tamoxifene blocca direttamente i recettori degli estrogeni sulle cellule ed è spesso usato nelle donne in pre-menopausa. Gli inibitori dell’aromatasi (come Letrozolo o Anastrozolo) impediscono invece la produzione stessa degli estrogeni nei tessuti periferici e sono lo standard di cura per le donne in post-menopausa.
